Table of Contents
Pada artikel ini, kita akan membahas pengertian unsur secara detail dan lengkap. Unsur adalah komponen dasar yang membentuk segala substansi di alam semesta. Konsep unsur sangat penting dalam ilmu kimia dan fisika, karena membantu kita memahami struktur materi dan reaksi kimia.
Unsur terdiri dari atom, yang merupakan unit terkecil dari materi yang masih dapat mempertahankan sifat-sifat kimiawi dan fisika dari unsur tersebut. Atom terdiri dari inti yang terdiri dari proton dan neutron, serta elektron yang berputar di sekitar inti. Ada 118 unsur yang telah teridentifikasi dalam tabel periodik, termasuk unsur-unsur yang ditemukan di alam dan yang telah disintesis secara buatan di laboratorium.
Pengertian Unsur
Pada sesi ini, kita akan mendefinisikan unsur secara rinci. Unsur adalah zat murni yang terdiri dari atom-atom yang memiliki nomor atom yang sama. Setiap unsur memiliki sifat-sifat khas yang membedakannya dari unsur lainnya. Unsur-unsur ini membentuk dasar bagi semua zat di alam semesta.
Unsur dapat ditemukan dalam berbagai wujud, baik dalam bentuk padat, cair, atau gas, tergantung pada suhu dan tekanan. Misalnya, oksigen adalah unsur yang umumnya ditemukan dalam bentuk gas di atmosfer, sedangkan besi adalah unsur yang sering ditemukan dalam bentuk padat sebagai logam.
Melalui studi tentang unsur, kita dapat mempelajari sifat-sifat fisika dan kimiawi yang unik dari setiap unsur. Sifat-sifat ini mencakup titik lebur, titik didih, massa atom, keelektronegatifan, dan banyak lagi. Pemahaman tentang unsur sangat penting dalam memahami berbagai fenomena alam, seperti reaksi kimia, pembentukan senyawa, dan sifat-sifat materi di sekitar kita.
Sejarah dan Perkembangan Pemahaman tentang Unsur
Pemahaman tentang unsur telah berkembang sejak zaman kuno. Pada zaman dahulu, manusia telah mengenal beberapa unsur tanpa menyadari konsep modern tentang atom. Misalnya, emas dan perak telah dikenal dan digunakan oleh peradaban kuno sebagai logam berharga.
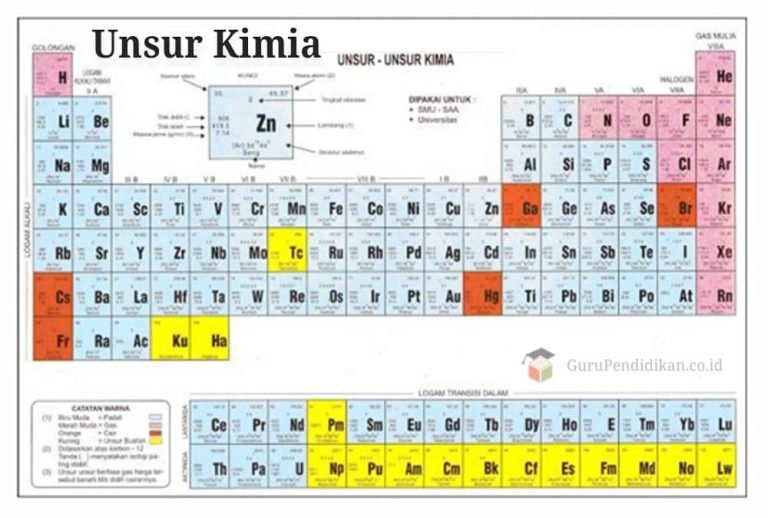
Pada abad ke-18 dan ke-19, para ilmuwan mulai melakukan penelitian yang lebih sistematis tentang unsur-unsur. Penemuan dan isolasi unsur-unsur baru menjadi fokus utama para peneliti. Pada tahun 1869, Dimitri Mendeleev mengembangkan tabel periodik yang mengatur unsur-unsur berdasarkan sifat-sifatnya. Tabel periodik ini menjadi fondasi bagi pemahaman modern tentang unsur.
Sejak itu, perkembangan teknologi dan penelitian ilmiah telah memungkinkan identifikasi dan sintesis unsur-unsur baru. Ilmuwan terus menggali lebih dalam untuk memahami sifat-sifat dan reaktivitas unsur, serta mengembangkan aplikasi praktis mereka dalam berbagai bidang kehidupan.
Jenis-jenis Unsur
Selanjutnya, kita akan membahas jenis-jenis unsur yang ada. Unsur-unsur dibagi menjadi beberapa kategori berdasarkan sifat-sifatnya. Klasifikasi yang umum digunakan adalah unsur logam, non-logam, dan gas mulia.
Unsur Logam
Unsur logam adalah unsur yang umumnya memiliki sifat-sifat seperti konduktivitas listrik dan panas yang baik, kilap logam, dan keuletan. Beberapa contoh unsur logam meliputi besi, tembaga, seng, aluminium, dan emas. Logam digunakan dalam berbagai aplikasi, seperti pembuatan peralatan elektronik, konstruksi, dan industri otomotif.
Unsur Non-logam
Unsur non-logam tidak memiliki sifat logam seperti kilap dan konduktivitas listrik yang baik. Sebaliknya, unsur non-logam cenderung rapuh, tidak mengkilap, dan memiliki sifat isolator. Contoh unsur non-logam meliputi oksigen, nitrogen, karbon, dan belerang. Beberapa unsur non-logam memiliki peran penting dalam kehidupan, seperti oksigen yang diperlukan untuk bernapas.
Gas Mulia
Gas mulia, juga dikenal sebagai unsur inert, adalah unsur yang sangat stabil dan kurang reaktif secara kimia. Unsur ini termasuk helium, neon, argon, kripton, xenon, dan radon. Karena sifat mereka yang inert, gas mulia sering digunakan dalam aplikasi yang memerlukan lingkungan yang tidak reaktif, seperti pencahayaan neon dan pengisian lampu pijar.
Sifat-sifat Unsur
Pada sesi ini, kita akan menjelaskan sifat-sifat kimiawi dan fisika yang dimiliki oleh unsur-unsur. Beberapa sifat kimiawi yang umumnya diamati adalah daya oksidasi, reaktivitas, dan keelektronegatifan. Sementara itu, sifat fisika meliputi titik lebur, titik didih, massa atom, dan banyak lagi.
Sifat Kimiawi
Daya oksidasi adalah kemampuan suatu unsur untuk bereaksi dengan oksigen atau mengalami oksidasi. Unsur yang memiliki daya oksidasi tinggi cenderung bereaksi lebih mudah dengan oksigen. Contohnya adalah logam alkali seperti natrium dan kalium, yang bereaksi dengan sangat kuat ketika terpapar udara.
Reaktivitas adalah kemampuan suatu unsur untuk bereaksi dengan unsur lain dan membentuk senyawa baru. Unsur yang sangat reaktif cenderung bereaksi dengan mudah dengan unsur lainnya. Contohnya adalah fluorin, yang merupakan unsur paling reaktif dalam tabel periodik.
Kelektronegatifan adalah kemampuan suatu unsur untuk menarik elektron dalam ikatan kimia. Unsur yang memiliki kelektronegatifan tinggi cenderung menarik elektron dengan kuat, sementara unsur dengan kelektronegatifan rendah cenderung kehilangan elektron. Contohnya adalah fluorin yang memiliki kelektronegatifan tertinggi dalam tabel periodik.
Sifat Fisika
Titik lebur adalah suhu di mana sebuah unsur berubah dari wujud padat menjadi wujud cair. Setiap unsur memiliki titik lebur yang khas, yang dipengaruhi oleh kekuatan ikatan antar atom-atomnya. Misalnya, titik lebur besi adalah sekitar 1535 derajat Celsius.
Titik didih adalah suhu di mana sebuah unsur berubah dari wujud cair menjadi wujud gas. Seperti titik lebur, tiap unsur memiliki titik didih yang unik. Misalnya, titik didih air adalah 100 derajat Celsius.
Massa atom adalah massa relatif dari sebuah atom unsur dibandingkan dengan massa 1/12 atom karbon-12. Massa atom digunakan untuk mengukur jumlah materi dalam skala atom. Misalnya, massa atom hidrogen adalah sekitar 1,008 unit massa atom.
Periode dan Golongan dalam Tabel Periodik
Tabel periodik mengatur unsur-unsur berdasarkan periode dan golongan. Pada sesi ini, kita akan membahas apa yang dimaksud dengan periode dan golongan dalam tabel periodik. Kita juga akan menjelaskan mengapa susunan unsur dalam tabel periodik sangat penting dalam mempelajari sifat-sifat unsur.
Periode dalam Tabel Periodik
Periode adalah baris horizontal dalam tabel periodik yang mengelompokkan unsur-unsur berdasarkan jumlah kulit elektron yang dimilikinya. Tabel periodik modern memiliki tujuh periode, yang mewakili jumlah kulit elektron dari 1 hingga 7. Misalnya, periode pertama terdiri dari unsur-unsur yang hanya memiliki satu kulit elektron,seperti hidrogen dan helium. Setiap periode dalam tabel periodik memiliki pola tertentu dalam sifat-sifat fisika dan kimianya.
Periode pertama terdiri dari unsur-unsur yang memiliki struktur elektron yang paling sederhana. Seiring kita bergerak ke periode yang lebih tinggi, jumlah elektron dalam kulit terluar meningkat, yang mempengaruhi sifat-sifat kimia unsur tersebut. Periode terakhir, yaitu periode ketujuh, adalah periode yang paling panjang dan mencakup unsur-unsur dengan tingkat kompleksitas elektronik tertinggi.
Golongan dalam Tabel Periodik
Selain periode, unsur-unsur dalam tabel periodik juga dikelompokkan menjadi golongan berdasarkan kesamaan sifat kimia mereka. Terdapat 18 golongan dalam tabel periodik, yang diberi nomor golongan dari 1 hingga 18. Unsur-unsur dalam golongan yang sama memiliki pola yang serupa dalam sifat-sifat fisika dan kimia mereka.
Beberapa contoh golongan dalam tabel periodik termasuk golongan logam alkali (golongan 1), golongan logam alkali tanah (golongan 2), dan golongan halogen (golongan 17). Setiap golongan memiliki karakteristik khas yang mempengaruhi sifat-sifat unsur-unsur di dalamnya.
Susunan unsur dalam tabel periodik sangat penting dalam mempelajari sifat-sifat unsur karena memperlihatkan pola dan tren yang terjadi. Pola periodik mengungkapkan perubahan berulang dalam sifat-sifat fisika dan kimia saat kita bergerak melintasi periode. Tren periodik, seperti peningkatan keelektronegatifan atau ukuran atom, dapat diamati saat kita bergerak ke bawah golongan dalam tabel periodik.
Dengan memahami susunan unsur dalam tabel periodik, kita dapat memprediksi sifat-sifat unsur yang belum diketahui dan memahami hubungan antara unsur-unsur yang berbeda. Tabel periodik menjadi alat yang sangat berguna dalam ilmu kimia dan digunakan dalam berbagai aplikasi, mulai dari penelitian laboratorium hingga industri dan teknologi.
Reaksi Kimia antar Unsur
Unsur-unsur dapat bereaksi satu sama lain membentuk senyawa kimia. Pada sesi ini, kita akan menjelaskan bagaimana reaksi kimia antar unsur terjadi. Kita akan membahas konsep ikatan kimia dan bagaimana unsur-unsur saling berbagi atau mentransfer elektron untuk membentuk senyawa baru.
Ikatan Kimia
Ikatan kimia adalah gaya tarik antara atom-atom dalam senyawa kimia. Terdapat beberapa jenis ikatan kimia, termasuk ikatan kovalen, ikatan ionik, dan ikatan logam. Jenis ikatan yang terbentuk bergantung pada sifat-sifat elektron dari unsur yang bereaksi.
Ikatan kovalen terjadi ketika dua atau lebih atom saling berbagi pasangan elektron. Ini sering terjadi antara unsur non-logam. Misalnya, dalam molekul air (H2O), oksigen dan hidrogen saling berbagi elektron untuk membentuk ikatan kovalen yang kuat.
Ikatan ionik terjadi ketika satu atau lebih elektron ditransfer dari satu atom ke atom lain, sehingga terbentuk ion positif dan ion negatif. Ini sering terjadi antara logam dan non-logam. Contohnya adalah natrium klorida (NaCl), di mana natrium melepaskan satu elektron untuk membentuk ion Na+ dan klorin menerima elektron tersebut untuk membentuk ion Cl-.
Ikatan logam terjadi ketika sekelompok atom logam saling berbagi elektron yang terdelokalisasi di sepanjang struktur kristal. Ini menyebabkan logam memiliki sifat konduktivitas listrik yang baik. Contoh ikatan logam adalah dalam logam seperti tembaga dan besi.
Reaksi Antara Unsur
Reaksi kimia antara unsur dapat menghasilkan pembentukan senyawa baru. Ketika unsur-unsur bereaksi, ikatan kimia dipecah dan ikatan baru terbentuk untuk membentuk struktur molekul yang berbeda.
Contoh reaksi antara unsur adalah reaksi antara hidrogen dan oksigen untuk membentuk air. Dalam reaksi ini, dua atom hidrogen (H) bereaksi dengan satu molekul oksigen (O2) untuk membentuk dua molekul air (H2O). Reaksi ini melibatkan pembentukan ikatan kovalen antara atom-atom hidrogen dan oksigen.
Reaksi kimia antara unsur juga dapat melibatkan transfer elektron, seperti dalam reaksi antara logam dan non-logam. Misalnya, reaksi antara natrium (Na) dan klorin (Cl) menghasilkan pembentukan natrium klorida (NaCl). Dalam reaksi ini, natrium melepaskan satu elektron untuk membentuk ion Na+, sementara klorin menerima elektron tersebut untuk membentuk ion Cl-. Ikatan ionik terbentuk antara ion Na+ dan Cl-.
Reaksi kimia antara unsur-unsur memiliki peran penting dalam berbagai sistem alam, seperti reaksi kimia dalam tubuh manusia atau dalam proses pembentukan senyawa dalam industri kimia. Pemahaman tentang bagaimana unsur-unsur bereaksi dan membentuk senyawa baru memberikan wawasan yang berharga dalam ilmu kimia dan dapat diterapkan dalam berbagai aplikasi praktis.
Unsur Penting dalam Kehidupan
Beberapa unsur sangat penting bagi kehidupan di Bumi. Pada sesi ini, kita akan menyoroti beberapa unsur yang esensial untuk makhluk hidup, seperti karbon, hidrogen, oksigen, nitrogen, dan fosfor. Kita akan menjelaskan peran penting mereka dalam molekul biologis dan reaksi kimia dalam tubuh kita.
Karbon
Karbon adalah unsur yang paling penting dalam kehidupan. Karbon merupakan komponen utama semua makhluk hidup dan membentuk kerangka struktural dalam molekul biologis seperti protein, lemak, dan karbohidrat. Selain itu, karbon juga merupakan dasar bagi senyawa organik yang memiliki peran penting dalam berbagai reaksi kimia dalam tubuh kita.
Hidrogen
Hidrogen adalah unsur yang paling melimpah dalam alam semesta. Hidrogen terlibat dalam berbagai reaksi kimia dan merupakan komponen utama dalam air (H2O) dan senyawa organik seperti asam amino dan asam nukleat. Hidrogen juga digunakan dalam produksi energi, seperti dalam reaksi nuklir di matahari yang menghasilkan energi surya.
Oksigen
Oksigen adalah unsur yang penting bagi kehidupan karena berperan dalam proses pernapasan. Oksigen membantu tubuh menghasilkan energi dengan membakar makanan dalam proses metabolisme. Selain itu, oksigen juga terlibat dalam berbagai reaksi kimia dalam tubuh yang mendukung fungsi organ dan sistem tubuh yang sehat.
Nitrogen
Nitrogen adalah unsur yang penting dalam pembentukan protein dan asam nukleat, yang merupakan komponen utama dalam DNA dan RNA. Nitrogen juga merupakan komponen penting dalam atmosfer Bumi dan berperan dalam siklus nitrogen, di mana nitrogen diubah menjadi bentuk yang dapat digunakan oleh tanaman dan makhluk hidup lainnya.
Fosfor
Fosfor adalah unsur yang penting dalam molekul biologis seperti DNA, RNA, dan ATP (adenosin trifosfat). ATP adalah molekul yang digunakan oleh sel untuk menyimpan dan mentransfer energi. Fosfor juga merupakan komponen utama dalam struktur tulang dan gigi manusia.
Unsur-unsur ini merupakan bagian integral dari kehidupan dan memainkan peran penting dalam berbagai proses biologis. Pemahaman tentang peran unsur-unsur ini dalam tubuh manusia dan organisme lainnya memberikan wawasan yang berharga dalam bidang biokimia dan ilmu kehidupan.
Unsur Langka dan Radioaktif
Beberapa unsur sangat langka dan hanya ditemukan dalam jumlah yang sangat kecil di alam. Pada sesi ini, kita akan membahas unsur-unsur langka seperti emas, perak, dan platinum. Kita juga akan menjelaskan apa yang dimaksud dengan unsur radioaktif dan mengapa mereka memiliki sifat yang unik.
Unsur Langka
Unsur langka adalah unsur yang memiliki kelimpahan yang sangat rendah di Bumi. Mereka sering ditemukan dalam bentuk bijih yang tersebar dan sulit diekstraksi. Contoh unsur langka termasuk emas, perak, platinum, dan uranium. Unsur-unsur ini memiliki sifat-sifat yang membuatnya berharga dan sangat dicari dalam industri perhiasan, elektronik, dan industri lainnya.
Emas adalah salah satu unsur langka yang paling terkenal. Emas digunakan dalam perhiasan, sebagai logam konduktor dalam elektronik, dan dalam industri kimiawi. Perak juga memiliki kelimpahan yang relatif rendah dan digunakan dalam perhiasan, fotografi, dan industri elektroplating. Platinum, dengan sifat keahanannya yang tinggi, digunakan dalam produksi kendaraan dan dalam industri kimia.
Unsur Radioaktif
Unsur radioaktif adalah unsur yang mengalami peluruhan radioaktif, yaitu pelepasan partikel-partikel radiasi. Peluruhan radioaktif terjadi ketika inti atom tidak stabil dan berusaha mencapai kestabilan. Inti atom dapat melepaskan partikel-partikel alfa, beta, atau radiasi gamma selama proses peluruhan ini.
Unsur radioaktif memiliki sifat unik yang digunakan dalam berbagai aplikasi, seperti dalam bidang kedokteran, industri, dan penelitian. Misalnya, isotop radioaktif iodin (I-131) digunakan dalam terapi radiasi untuk mengobati kanker tiroid, sementara isotop radioaktif kobalt-60 digunakan dalam terapi radiasi untuk mengobati kanker.
Beberapa unsur radioaktif juga digunakan dalam penanggalan radiometrik untuk menentukan usia benda-benda arkeologi dan geologi. Metode penanggalan ini memanfaatkan peluruhan radioaktif unsur-unsur tertentu dan perhitungan berdasarkan laju peluruhan tersebut.
Unsur langka dan radioaktif memiliki sifat-sifat yang unik dan berharga dalam berbagai aplikasi. Meskipun langka, unsur-unsur ini memainkan peran penting dalam industri dan penelitian, serta memberikan wawasan yang berharga dalam pemahaman tentang struktur atom dan sifat-sifat materi.
Unsur dalam Industri dan Teknologi
Unsur-unsur memiliki berbagai aplikasi dalam industri dan teknologi. Pada sesi ini, kita akan mengeksplorasi penggunaan unsur-unsur dalam berbagai bidang seperti elektronik, katalisis, energi, dan pengobatan. Kita akan memberikan contoh konkrit tentang bagaimana unsur-unsur digunakan dalam masyarakat modern.
Elektronik
Unsur-unsur memiliki peran penting dalam industri elektronik. Misalnya, silikon (Si) digunakan sebagai bahan dasar dalam pembuatan chip dan komponen semikonduktor. Logam-logam seperti tembaga (Cu) dan aluminium (Al) digunakan dalam kabel dan koneksi elektronik. Unsur-unsur langka seperti emas (Au) dan platinum (Pt) digunakan dalam kontak elektrik yang tahan karat dan konduktor yang baik.
Katalisis
Unsur-unsur juga digunakan sebagai katalis dalam berbagai reaksi kimia industri. Katalis adalah zat yang mempercepat laju reaksi kimia tanpa ikut bereaksi secara permanen. Beberapa logam transisi seperti besi (Fe), nikel (Ni), dan platina (Pt) digunakan sebagai katalis dalam produksi amonia, polimer, dan bahan kimia lainnya. Katalis juga digunakan dalam industri minyak dan gas untuk meningkatkan efisiensi proses pemurnian dan konversi.
Energi
Unsur-unsur memiliki peran penting dalam produksi energi. Misalnya, uranium (U) digunakan sebagai bahan bakar dalam reaktor nuklir untuk menghasilkan energi listrik. Sel surya menggunakan silikon (Si) sebagai bahan dasar dalam mengubah energi matahari menjadi energi listrik. Logam-logam seperti kobalt (Co), nikel (Ni), dan litium (Li) digunakan dalam pembuatan baterai untuk penyimpanan energi.
Pengobatan
Unsur-unsur juga memiliki peran penting dalam bidang pengobatan. Misalnya, teknetium-99m (99mTc) adalah isotop radioaktif yang digunakan dalam pemindaian diagnostik untuk mendeteksi berbagai kondisi medis. Logam-logam seperti platina (Pt) dan iridium (Ir) digunakan dalam terapi kanker dengan metode radioterapi. Unsur-unsur lain seperti besi (Fe), kalsium (Ca), dan kalium (K) juga penting dalam fungsi tubuh dan pembentukan tulang.
Unsur-unsur memiliki peran vital dalam berbagai industri dan teknologi. Penggunaan mereka dalam elektronik, katalisis, energi, dan pengobatan memungkinkan kemajuan dalam berbagai bidang kehidupan kita. Penelitian terus dilakukan untuk mengembangkan dan memanfaatkan unsur-unsur secara lebih efisien dan berkelanjutan.
Contoh-contoh Unsur dalam Kehidupan Sehari-hari
Pada sesi terakhir, kita akan memberikan beberapa contoh unsur yang sering kita temui dalam kehidupan sehari-hari. Kita akan menjelaskan bagaimana unsur-unsur seperti besi, kalsium, dan aluminium digunakan dalam berbagai objek dan produk yang kita gunakan setiap hari.
Besi
Besi (Fe) adalah unsur yang sangat umum dan penting dalam kehidupan sehari-hari. Besi digunakan dalam konstruksi untuk pembuatan bangunan, jembatan, dan kendaraan. Selain itu, besi juga digunakan dalam pembuatan alat-alat rumah tangga seperti panci, pisau, dan kunci.
Kalsium
Kalsium (Ca) adalah unsur yang terkandung dalam tulang dan gigi manusia. Kalsium juga penting dalam kontraksi otot, pembekuan darah, dan fungsi saraf yang normal. Kita dapat mendapatkan kalsium dari makanan seperti susu, keju, dan sayuran hijau.
Aluminium
Aluminium (Al) adalah unsur yang ringan, kuat, dan tahan karat. Aluminium digunakan dalam pembuatan berbagai produk, seperti kaleng minuman, kerangka jendela, dan komponen kendaraan. Kelebihan aluminium adalah dapat didaur ulang, yang membuatnya menjadi pilihan yang ramah lingkungan.
Perak
Perak (Ag) adalah unsur yang memiliki sifat konduktor yang sangat baik. Perak digunakan dalam industri elektronik, seperti dalam pembuatan kabel, kontak elektrik, dan komponen semikonduktor. Perak juga digunakan dalam perhiasan dan benda dekoratif karena kilauannya yang indah.
Karbon
Karbon (C) adalah unsur yang penting dalam senyawa organik dan hidrokarbon. Karbon membentuk kerangka struktural dalam senyawa seperti protein, lemak, dan karbohidrat. Karbon juga terkandung dalam produk-produk sehari-hari seperti plastik, karet, dan bahan bakar fosil.
Unsur-unsur ini adalah contoh-contoh unsur yang sering kita temui dalam kehidupan sehari-hari. Penggunaan unsur-unsur ini dalam berbagai produk dan aplikasi menggambarkan betapa pentingnya unsur-unsur dalam kehidupan kita.